浏览次数:536 发布时间:2026-04-17 10:30:32
摘要
生物制造作为实现绿色低碳和可持续发展的重要技术路径,正沿着“原料—技生物制造正成为全球经济增长的新引擎,备受世界主要经济体重视。梳理了生物制造的概念内涵,从科技发展和战略举措2方面分析研判国际竞争态势,总结了中国在科技成果、创新平台及产业发展等方面的进展。针对中国生物制造产业面临的4大挑战:基础共性技术创新能力薄弱、可持续低成本原料开发不足、生物制造装备自主性和系统性欠缺、产业人才短缺,提出相关建议。未来,应面向中国粮食安全、能源安全等重大战略需求,通过强化政策协同和技术革新,夯实基础研究,突破关键核心技术瓶颈,加速推动科技成果产业化,着力建设多元化、高水平的科技人才梯队,为生物制造产业高质量发展提供科技支撑。
生物制造蕴含巨大潜力,有望成为全球经济增长的新引擎。麦肯锡全球研究院在《生物革命:正在重塑经济、社会与生活的创新》(《The bio revolution: Innovations transforming economies, societies, and our lives》)报告中指出,理论上,目前全球约60%的产品(包括木材、动物制品、塑料、燃料等)可通过生物制造方式替代或生产。波士顿咨询公司在《合成生物学即将颠覆产业格局》(《Synthetic biology is about to disrupt your industry》)报告中预测,到2030年,合成生物学将全面渗透传统制造业,从健康美妆、医疗器械、电子到化工、纺织、水务管理再到采矿、电力和建筑等,其产值有望达到30万亿美元,展现出极为广阔的应用前景。
中国将生物制造作为新质生产力的核心代表和6大未来产业之一,全力打造为驱动国家经济高质量发展的强劲新引擎。“十五五”时期将是生物科技加速演进、生物制造产业迅猛发展的重要机遇期,也是实现中国高水平科技自立自强的重要关口。抓住新一轮科技创新发展机遇,综合研判生物制造科技发展态势,深入剖析中国生物制造产业高质量发展面临的主要需求及问题,对培育新增长点和推动传统产业转型升级具有重要意义。
1 生物制造概念的内涵
目前,国际上尚未就“生物制造”的定义与范畴形成统一共识。欧盟与美国基于不同的产业政策与科技治理逻辑,形成了2种代表性的界定模式。
欧盟将生物制造视为生物技术创新的工业化实现途径,其核心是通过生物资源转化生产化学品、材料及能源等。该定义覆盖全产业链范畴,涵盖农业、林业、渔业、食品加工、纸浆造纸等基础领域,并延伸至化工、生物技术和能源产业的关键环节。美国将生物制造定义为“通过生物系统(含植物、微生物及其分子组分)在工业规模实现产品制造的过程”,其核心主要聚焦于“以生命科学与生物技术创新为驱动的先进生物制造”。相较于欧盟,美国生物制造行业范围更窄,不包括烟草制造、皮革制品、木材加工、纸制品、家具及服装等传统行业。
国内对于生物制造的界定主要呈现双维视角。在技术范式维度,定义为以合成生物学、人工智能等前沿技术驱动的先进制造方式,其核心从传统发酵迭代至合成生物学、生物计算等新一代技术体系;在产业范畴维度,强调其作为绿色制造核心载体的定位,在工业减排、生物基材料替代等场景持续深化应用。尽管上述2种维度侧重不同,但均将生物制造视为未来产业升级和可持续发展的重要驱动力。
2 国际发展形势2.1 生物制造领域科技发展趋势近年来,生物制造底层技术持续突破,推动行业迈向精准、高效和规模化。底盘细胞改造能力显著提升,大肠杆菌、枯草芽孢杆菌、酿酒酵母等模式微生物优化深入,极端微生物如嗜盐菌、嗜热菌等展现出作为下一代细胞工厂的潜力。基因编辑工具迭代与脱氧核糖核酸(deoxyribo nucleic acid,DNA)合成高通量化大幅提升生物功能设计精度与效率,人工基因组合成范围已扩展至真核生物,染色体级构建技术成为焦点。合成生物学与人工智能技术深度耦合,加速基因功能解析、代谢路径优化等研究,精准模拟、预测基因表达与调控网络,并贯穿设计—构建—测试全流程。
工艺绿色低碳化日益受到关注,推动生物炼制向更加清洁、可持续模式转型。生物制造绿色化进程加速,其发展正从第一代(淀粉/油脂)、第二代(木质纤维素等非粮废弃物)原料,迈向以CO2及其衍生物(气体碳源)为原料的第三代。同时,副产物综合利用理念从“末端治理”转向“价值再造”。通过厌氧消化、水热液化或级联发酵等技术,将菌渣、废弃发酵液等转化为沼气、有机肥或高价值化学品,形成“原料−产品−副产物−再生资源”的绿色循环产业链。下游分离提取技术也向高效精细化发展,超临界萃取、膜分离、连续色谱等先进方法应用于药物与高值化学品精制,大幅提高产物回收率与纯度。
合成生物制造正深刻变革物质生产方式,逐步实现技术成熟与市场应用。该技术利用生物资源在温和条件下(常温、常压、水相)高效生产产品,推动化工原料与生产过程的绿色替代,加速产业从石化基向生物基转型。其应用前景广阔,覆盖医药、农业、食品、化工、材料及能源等多个领域。目前,在大宗发酵产品、可再生化学与聚合材料、精细与医药化学品、天然产物、未来农产品等关键领域,重大产品的合成生物制造持续取得突破。预计未来数年,生物制造将在更多领域实现更广泛的应用与更深层次的创新。
2.2 主要国家生物制造战略举措1) 美国。美国强调充分利用先进生物技术和生物制造的潜力,以巩固其全球生物制造领域的领导地位和竞争力。自2022年起,美国密集发布了一系列生物制造战略政策。2022年9月,美国总统拜登签署第14081号行政命令——《关于推进生物技术和生物制造创新以实现可持续、安全和可靠的美国生物经济的行政命令》(《Executive order on advancing biotechnology and biomanufacturing innovation for a sustainable, safe, and secure American bioeconomy》),系统规划了生物技术与生物制造的国家级发展蓝图,以应对卫生、气候变化、能源、粮食安全等方面的挑战。2023年3月,美国白宫科学和技术政策办公室发布《生物技术与生物制造宏大目标》(《Bold goals for U.S. biotechnology and biomanufacturing》)报告,设定了气候、食品与农业、供应链、人类健康和跨学科5大领域的发展目标;同月,美国国防部发布《生物制造战略》(《DoD releases biomanufacturing strategy》),通过技术合作、应用实践和生态系统建设3方面举措加速本土生物制造发展。
2) 欧盟。欧盟将生物制造视为工业转型的核心驱动力,通过系统性政策框架推动该领域发展,以实现经济竞争力和环境可持续发展。2018年10月,欧盟委员会发布《可持续、可循环的生物经济发展新战略》(《A new bioeconomy strategy for a sustainable Europe》),将扩大可再生资源利用列为优先方向,将废弃物、残渣等转化为高附加值产品、绿色化学品、饲料和纺织品;2023年3月,欧洲生物产业协会举办首届生物制造政策峰会,提出建立“欧洲生物制造路线图”;2024年3月,欧盟委员会发布《与自然构筑未来:促进欧盟的生物技术和生物制造》(《Building the future with nature: boosting biotechnology and biomanufacturing in the EU》)倡议,从科研创新、市场需求、监管、投融资、技能、标准、国际合作、人工智能技术应用等多个方面提出促进生物制造业发展的关键行动。
3) 其他国家。英国通过工程生物学引领生物制造业发展。2023年12月,英国科学、创新和技术部发布《工程生物学国家愿景》(《Government publishes £2 billion vision for engineering biology to revolutionise medicine, food and environmental protection》),宣布了一项未来10年投入20亿英镑的战略,旨在释放工程生物学颠覆性潜力,大力推进合成生物制造业的发展。
日本将生物制造和生物基产品列为核心支柱之一。2023年11月,日本经济产业省启动《生物制造革命推进专项研究开发计划》(《バイオものづくり革命推進事業研究開発計画を改訂しました》),旨在升级本土生物制造工艺并拓展全球市场,重塑产业竞争力。2024年6月,日本发布新版《生物经济战略》(《バイオエコノミー戦略》),打造融合生物技术、人工智能与数字技术的微生物与细胞设计平台,同步完善生物工厂等关键基础设施,全面释放生物制造的乘数效应。
3 中国生物制造发展现状与问题3.1 中国生物制造发展现状生物制造领域科技发展取得显著突破。近年来,国家实施了一批重大专项,如“合成生物学”“绿色生物制造”等国家重点研发计划专项,推动该领域迅猛发展。原创性研究成果不断涌现,包括人造单染色体真核细胞、CO2人工合成淀粉、工业尾气制饲料蛋白[、基于极端微生物的下一代工业生物技术等一系列里程碑式进展,标志着中国在该领域的科研质量、技术水平和国际影响力实现同步跃升。
生物制造创新平台不断完善。京津冀、长三角、粤港澳大湾区等重点区域陆续建成多个研究中心,显著拓展了研究网络并提升了整体创新能力。其中,合成生物学前沿科学中心聚焦前瞻性、战略性、前沿性基础研究;国家合成生物技术创新中心集核心技术研发、技术转移转化、企业培育、资本运营于一体,打造全链条创新平台;国家生物制造产业创新中心由国家级科研机构联合央企、国企和龙头民营企业共同建设,重点突破生物制造技术从实验室到产业化的关键环节。
生物制造产业链条日臻完善,并已形成显著的规模优势。其中,生物发酵作为基础产业,产品总量在全球处于领先地位,特别是大宗生物发酵产品的产量已占据全球约70%。据2025中国生物发酵产业技术大会相关数据显示,2024年生物发酵产品产量达3400万t,同比增长约5%;出口约881万t,同比增长约20%。在部分重大化工产品生物制造领域,中国已率先实现产业化,生物基塑料、生物基化学纤维、生物基橡胶等细分赛道产业化水平居全球前列。
3.2 中国生物制造发展面临的挑战与问题
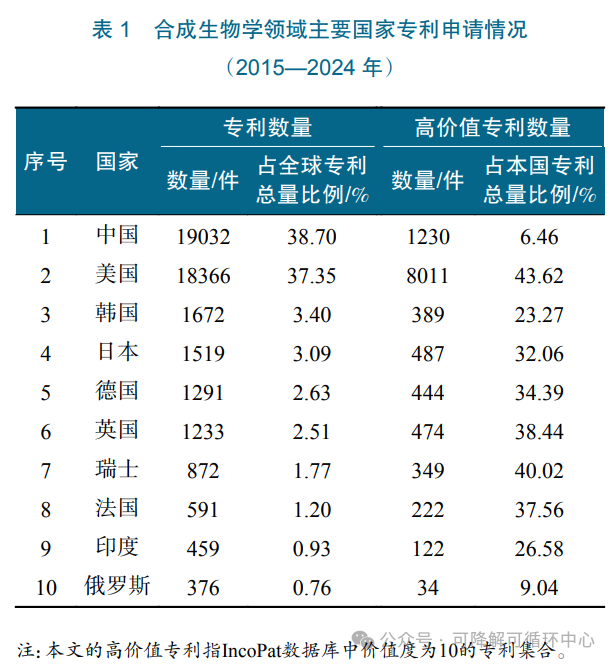
1) 基础共性技术创新能力不足。中国合成生物学关键使能技术落后于发达国家。波士顿咨询公司报告指出,在设计环节,二代测序技术中外处于并跑阶段,但三代测序技术国内起步较晚,呈快速追赶趋势;同时,国内高度依赖海外数据库及工具。在构建环节,中国起步较晚,DNA合成、基因编辑等技术虽处于快速追赶态势,但仍需要突破专利封锁。在测试环节,中外差距显著,国内以自动化机械辅助人工测试为主,而国外如美国银杏生物公司已实现百万级别的菌株筛选。在学习环节,国外在预测算法准确度、数据积累以及无注释预测算法等领域处于领先地位,国内整体处于发展早期。专利方面,虽然中国的专利申请总量位居全球首位(19032件,占比为38.7%),但高价值专利数量相对较少(1230件,占比为6.46%),仅为美国的约1/7(表1)。
工业菌种面临“两低一高”的严峻挑战。一是菌种改良效率低。国内发酵工业中广泛使用的菌种大多通过传统诱变育种方式获得,改良效率低且周期长。二是菌种性能水平低。传统菌种改良方法难以同时优化多个基因表达,难以培育出遗传稳定、适应性强的工业菌种。三是知识产权风险高。中国多个优势领域80%以上的工业菌种未经授权使用,存在严重的知识产权侵权风险。例如,氨基酸产量占全球总量的60%,但菌种自主率却不到5%。
部分高端酶制剂仍高度依赖进口。酶制剂产业属于知识密集型的高科技领域,技术门槛高、研发投入大且周期长。这些特点导致全球酶制剂市场长期呈现寡头垄断格局,美国、欧盟等国家(地区)的企业在高端发酵品领域占据技术垄断地位。目前,中国发酵工业的核心酶制剂超过75%仍需依赖国外供应。在农产品加工的关键环节,所需酶制剂大多依赖进口,而在食品酶和工业洗涤酶等高端领域,国外品牌也占据主导地位。
2) 可持续低成本原料开发不足。原料构成相对单一,过度依赖主粮。当前,中国生物制造产业的主要原料为淀粉,其中约90%的初始原料来源于玉米等粮食作物。以柠檬酸生产为例,每生产1 t柠檬酸需消耗约1.9 t玉米等粮食。此外,在生物基塑料、生物基化学纤维等众多生物基材料的生产过程中,玉米、小麦等同样是不可或缺的常用原料。长远来看,这种过度依赖粮食原料的模式不仅会引发“与民争粮、与畜争饲”的问题,也不利于原料供应的自主可控和产业链供应链的稳定,更不利于生物制造产业的可持续发展。
转向非粮生物质资源是降低粮食消耗的理想策略。一是中国农林废弃物资源丰富,如农作物秸秆年产量约8.6亿t,但目前仍以就地还田为主,离田高值化利用尚处于起步阶段。二是工业副产碳源潜力巨大,如生物柴油副产粗甘油、制糖工业的糖蜜以及工业尾气等,量大价廉却普遍被低值处置。三是一碳资源来源广泛且成本低廉,是下一代绿色制造的潜在原料,但其生物转化技术仍处于实验室验证阶段。
非粮生物质资源大规模产业化仍面临诸多关键瓶颈。一是原料转化效率低。木质纤维素结构致密、组分复杂,酶解效率远低于淀粉基粮食原料,导致糖化成本高昂。二是过程抑制物多。预处理液及转化体系中积累的毒性物质会抑制微生物活性,降低产物得率。三是一碳生物技术的商业化条件尚不成熟。气体碳源的生物固定与转化仍处于实验室阶段,存在碳捕集效率低、放大规律不明等问题,与工业化需求差距显著。
3) 生物制造装备自主性和系统性不足。在基础研究端,部分高端科研仪器高度依赖进口,影响自主创新,威胁科技安全。2022年,色谱仪、质谱仪和光谱仪的进口率(采购金额占比)分别达83%、81%和75%。部分核心零部件如色谱柱、离子源、质量分析器等技术壁垒高,国产化程度较低。
在生产端,中国在原材料、加工、配件、检测等细分领域,尤其生物反应器、生物分离介质、仪器仪表等关键设备和材料方面,与国际先进水平存在差距。同时,在分离提取水平、检测评价技术、智能控制流程等方面存在不足,部分核心仪器依赖进口。
中国生物制造行业尚缺完备的装备与技术体系。“十四五”期间,中国生物制造行业以产品为核心,启动了一批中试与示范工程,但在工程装备成套系统等方面,仍未形成完善的评价标准。
4) 生物制造产业面临人才短缺。高端复合型人才储备薄弱。生物制造作为高度跨学科领域,亟需具备生物学、化学、工程学及计算机科学等多学科背景的专业人才。例如,底盘菌种创制高度依赖生物学、遗传学、发酵工程等多学科交叉人才。然而,中国现有的人才结构及人才培养体系难以满足行业需求,导致显著的人才结构性短缺。此外,欧美国家凭借高薪酬和灵活政策持续虹吸全球顶尖智力资源,加剧了中国高端人才引进的挑战。
产教融合不够紧密导致人才培养与需求脱节。当前,高校学科设置与生物制造产业需求存在结构性失衡,研究生培养过度侧重上游菌种设计与理论研发,而中下游发酵工艺、工程放大等实践型课程薄弱,造成发酵及工程过程等环节的人才短缺。此外,产学研协同机制的不完善进一步制约了复合型人才培养和科研成果转化,具体表现为:对原材料成本等产业要素关注不足;过度强调论文和专利产出,忽视成果产业化价值;高校毕业生实操经验欠缺,难以满足岗位要求。
4 建议
4.1 统筹布局生物制造关键核心技术协同攻关
加强顶层设计与部门协同,统筹资源配置,借鉴国际经验并结合国情制定国家生物制造产业发展蓝图,明确可考核的发展目标与实施路径,为全链条发展提供系统性指导。聚焦生物制造领域重大基础问题、共性基础技术和关键核心技术,系统部署重大研究专项,夯实科技基础能力。
一是强化基础研究引领突破。拓宽底盘生物系统的应用范围(微生物拓展至动植物及酶制剂领域),实现生物制造技术全覆盖;发展新一代合成生物学和基因编辑技术,加速应用于核心菌种和酶制剂创新;深化工具赋能,推动人工智能与合成生物学深度融合,集成精密工程、自动化、大数据等技术,构建智能合成生物制造系统。二是实施基础能力建设专项。加快建设国家生物信息中心、独特菌种库,构建自主开源的生物数据计算平台,强化数据全流程整合与应用,完善数据治理体系。三是部署关键核心技术攻关专项。集中突破共性技术短板与“卡脖子”难题,重点攻克工业菌种、酶制剂、关键设备等核心技术。四是推进重大产品工程与应用。以国家重大战略需求为导向,实施生物制造赋能产业升级工程,推动其在工业、食品、能源等领域的规模化应用。
4.2 打造“非粮生物质资源高效、高值化利用+合成生物制造”新模式
强化可持续低成本原料开发,探索糖蜜、玉米浆等低成本生物质原料利用,加强木质纤维素等非粮生物质的规模化应用;推广绿氨等绿色可再生资源,重塑产业链布局,赋能边远地区成为生物制造中心;优化淀粉碳源产业链,为第二代、第三代生物制造技术的成熟应用奠定产业基础。
短期内,重点突破木质纤维素为原料的第二代生物制造技术。发展高效的非粮生物质预处理技术,提高酶或酸对纤维素、半纤维素的可及性和水解率;构建低成本、高效协同的复合酶解体系或酸解体系,实现木质纤维素向可发酵单糖的高效转化;开发适配非粮生物质特性的工业菌种,高效生产乳酸、乙醇等化学品及生物燃料。
未来,布局以一碳化合物(CO2、CH4、CO等)为原料的第三代生物制造技术。针对生物利用效率低和途径匮乏问题,构建一碳化合物高效利用工程菌株,优化蛋白质设计以提升固碳和转化能力;设计生物转化或生物−化学耦合路线,实现一碳化合物固定与高效利用;开发适配气体转化的生物反应器及智能控制系统,提升一碳化合物利用率和碳原子经济性。
4.3 加强生物制造装备系统集成与国产化应用
加速推进生物制造领域关键仪器设备研发。通过集成生物过程工程、材料科学、计算模拟和自动化控制等技术,重点开发高效可控、适应多场景需求的生物反应器(如微泡式、自吸式、超大规模式),强化成套设备系统的示范应用与工艺优化。突破高灵敏度检测器、自动化样品处理模块等关键技术,实现生产全流程的自动化与智能化,提升系统稳定性和效率。
构建产学研联合攻关机制。建立产学研协同创新平台,整合高校、科研院所和企业资源,开展装备关键技术联合攻关、科技成果转化和人才培养,通过订单式研发、战略联盟和共建实体等模式,确保装备研发与市场需求紧密结合;健全装备与技术体系评价标准,加速创新成果产业化落地。
通过政策激励和资金支持,推动国产装备在终端用户的规模化应用,并加速性能迭代,增强产业自主可控能力。鼓励高校及科研机构优先采购国产高端生命科学仪器及生物制造装备,降低关键设备进口依赖;建立仪器共享服务平台,通过开放课题和数据共享提高设备利用率,形成覆盖基础研究到产业转化的全周期服务网络。
4.4 强化协同以加速科技成果产业化
构建贯通上下游的生物制造产业生态系统,整合资源、打破创新链与产业链壁垒,通过集群化发展促进上下游协作,实现产业链整体升级。
在基础研究到应用研究环节,打造概念验证平台,推动科研成果实现从概念到验证的“0到1”突破。汇聚关键资源和技术要素,以原创底层技术为基石,搭建满足基础或应用研究共性技术平台,特别是高通量筛选、基因编辑、理性设计等合成生物学平台,为生物制造领域的创新提供坚实的技术基础,推动科技成果向实际应用的快速转变。
在中试到产业化环节,建设一批智能化、定制化的一站式生物制造中试基地,推动科研成果实现从“1到100”的中试转化。聚焦生物制造重点产业,如食品及添加剂、化工及能源、生物制药、生物基材料、非粮生物质原料利用等,集中突破大规模发酵、分离纯化等工程化瓶颈,搭建满足产业共性需求的技术平台,提供标准化的技术支持和共享服务,降低研发成本和风险,加速科技成果转化为现实生产力。
4.5 建设多元化的生物制造科技人才梯队
加强生物制造领域跨学科人才培养。在高等院校设立“生物制造与合成生物学”等交叉学科专业,开发数据科学、人工智能应用等相关课程,确保学生掌握生物技术与数字技术的综合应用能力。推进联合培养与交换生计划,汇聚全球优质资源,引进先进理念与技术,构建多学科贯通的知识体系,培养兼具生物技术与数字技术能力的复合型人才。
建立生物制造高层次人才库,为人才培养与精准引才提供指引。实施国际人才引进计划,吸引顶尖国际人才加入中国生物制造产业,提升人才队伍国际化水平。重点培育具备前瞻性判断力、跨学科理解能力和大兵团作战组织能力的战略科学家;支持潜力突出的青年科技人才担纲领衔,形成优势互补的创新团队。
探索生物制造产学研协同育人新模式,着力培养应用型、工程化紧缺人才。支持高校、科研院所依托“产教联合体”“产业学院”“卓越工程师学院”等平台,深化生物制造领域院校企联合培养机制。通过校企共商培养方案、共建导师团队、共设实践基地,将产业需求融入人才培养全过程,重点强化工程实践能力与产业创新能力。